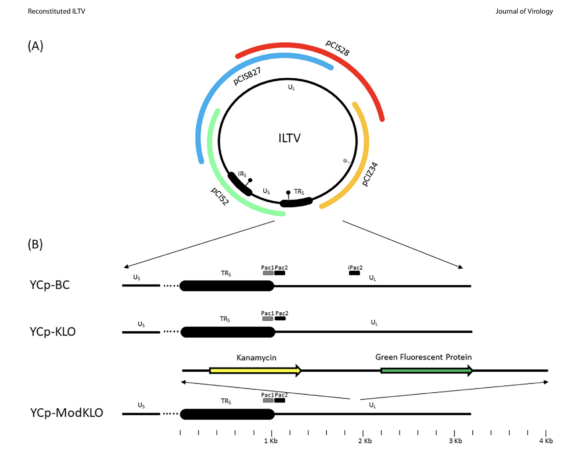
Según lo explicado en el texto, se reconstituyeron tres virus en células de riñón de pollo, similares a la cepa de referencia de ILT en un sistema de clonación conocido como cosmid/yeast centromeric plasmid (YCp). Posteriormente, se logró reconstituir un virus viable, lo que implica que esta plataforma podrá ser utilizada para desarrollar nuevas vacunas y más seguras contra esta enfermedad.
 El Dr. Loncoman respondió a algunas de las principales interrogantes en este tema.
El Dr. Loncoman respondió a algunas de las principales interrogantes en este tema.
- ¿Por qué los intentos previos de clonar el genoma completo del virus no habían sido exitosos?
“Previamente, se han empleado cromosomas artificiales bacterianos para clonar este virus, y una vez que se lograba clonar el genoma en este sistema, el genoma viral se volvía inestable y no se lograba reconstituir al virus viable posterior a su clonación.
El tamaño de un genoma para clonarlo es un factor importante, mientras más grande, más complejo. En este sentido, los herpesvirus poseen un genoma considerado como ‘extenso’ de aproximadamente 150 mil pares de bases de DNA de doble hebra. Una vez que se logra clonar un genoma viral, lo más relevante es poder reconstituir al virus nuevamente, es decir, recuperarlo completamente, junto a su capacidad de replicación, que cause un efecto citopático in vitro (daño celular) y enfermedad en su hospedador in vivo. Esta última parte es esencial para determinar que el sistema de clonamiento funciona correctamente”.
- ¿Existe la posibilidad de que, al igual que la gripe aviar, este virus se transmita a humanos?
“No existe evidencia de que este virus se pueda transmitir hacia o entre seres humanos. Sin embargo, este virus pertenece a la clasificación taxonómica de subfamilia Alphaherpesvirinae, a la que pertenecen virus que afectan a las personas como los que causan herpes bucal o labial, genital y el herpes zoster (varicela). Los virus que pertenecen a este grupo son considerados hospedador-especifico, es decir, son virus que han co-evolucionado junto a sus hospedadores para tener una relación virus-hospedador de tipo estable, predecible y específica”.
Vacunas mejoradas gracias a la modificación genética
Respecto a su impacto, la laringotraqueítis infecciosa alcanza un 100% de morbilidad, es decir, todas las aves de un galpón expuestas al virus se enferman, y entre un 30 a un 70% de las aves enfermas mueren, dependiendo del grado de virulencia del virus y de la respuesta inmune que genere el hospedador. Entre los signos que se observan en las aves enfermas están la disminución de la producción de huevos, estornudos, conjuntivitis, disnea (dificultad para respirar) y tos productiva sanguinolenta en los casos más severos.
Según lo explicado en el artículo, los resultados obtenidos tras el proceso de clonación dan cuenta de que los virus reconstituidos fueron capaces de causar enfermedad clínica en los animales experimentales, similar a lo que se observa en las aves infectadas naturalmente con virus de campo (virus sin clonar), lo que demuestra que los virus reconstituidos recuperan completamente sus capacidad de causar enfermedad.
En este contexto, el estudio realizado abre la puerta para el desarrollo de vacunas con mayores estándares de seguridad y eficacia permitiendo, además, comprender de mejor manera la función de cada uno de los genes presentes en el genoma viral, propiciando el desarrollo de vacunas.
- ¿Por qué las vacunas atenuadas y vectorizadas existentes no son eficaces?
“Las vacunas que actualmente existen y que son comercializadas en el mundo, incluyendo Chile, son principalmente vacunas vivas atenuadas que contienen al virus completo y que tienen la desventaja de revertir su virulencia. Es decir, una vez que la vacuna se aplica en un animal, el virus presente en la vacuna se replica y se transmite a otros pollos no vacunados causando enfermedad. Estos eventos de reversión han sido un problema y con esta nueva plataforma de clonamiento se podrían evaluar nuevas estrategias para producir nuevas vacunas, más seguras, que sean capaces de generar una respuesta inmune, pero no revertir.
Por otro lado, en Estados Unidos existen las vacunas vectorizadas. Estas vacunas son fabricadas con trozos del virus que causa la ILT. Sin embargo, estas vacunas no logran el mismo grado de protección contra la enfermedad. Por lo tanto, es imprescindible identificar el rol de cada uno de los genes que se encuentran en el genoma del virus y determinar con exactitud el rol de ellos en la respuesta inmune del hospedador y en el ciclo de infección”.
Laringotraqueítis infecciosa en Chile
La laringotraqueítis infecciosa es una enfermedad que está actualmente extendida por todo el mundo y en Chile su notificación es obligatoria.
Si bien nuestro país se caracteriza por tener disponible para su comercialización vacunas que se producen en Estados Unidos y Europa, estas no son consideradas seguras, ya que se ha detectado el virus de estas vacunas en aves de traspatio de pequeños productores que nunca habían sido inoculadas.
“Asimismo, otros investigadores de la UACh han detectado la presencia del material genético de este virus en aves silvestres. Estas evidencias sirven para que podamos tomar medidas de prevención y por supuesto contribuir al desarrollo de vacunas más seguras para el uso veterinario, independiente de si causan o no un impacto económico en la industria animal”, enfatizó el académico Carlos Loncoman.
Finalmente, cabe señalar que el grupo de investigación está integrado, además, por Stephen Spatz, Maricarmen García, Walter Fuchs, Jeremy Volkening, Teresa Ross, Sylva Riblet, Taejoong Kim, Nathan Likens y Thomas Mettenleiter.
El artículo completo puede ser revisado directamente en este enlace.